铜与浓硝酸反应后溶液呈绿色的原因主要是:反应过程中产生了大量的二氧化氮(NO₂)气体,二氧化氮部分溶解在溶液中,其黄色与铜离子(Cu²⁺)的蓝色混合,从而使溶液呈现出绿色。
铜与浓硝酸反应的化学方程式为:Cu + 4HNO₃(浓)=Cu (NO₃)₂ + 2NO₂↑ + 2H₂O。
虽然二氧化氮会与水发生反应(3NO₂ + H₂O = 2HNO₃ + NO),但在浓硝酸环境中,水分相对较少,一部分二氧化氮未发生水合,保持了原有的颜色。
需要注意的是,溶液的颜色还可能受到其他因素的影响,例如反应条件、溶液中其他物质的存在等。也有研究认为,可能是二氧化氮与水反应生成的亚硝酸,再结合铜离子生成铜的亚硝酸化合物,导致溶液呈绿色。
此外,如果对绿色溶液进行加热,会促使二氧化氮气体逸出,溶液中二氧化氮含量减少,颜色可能会变为蓝色;或者加入较多的水稀释,也可能使溶液颜色变回蓝色。
我们来看看下面探究性实验题
某小组进行铜与浓硝酸反应的实验后,观察到:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。小组成员试图探究溶液变绿的可能性。
(1)铜与浓硝酸反应的化学方程式为______。Cu + 4HNO₃(浓)=Cu (NO₃)₂ + 2NO₂↑ + 2H₂O
(2)甲同学推测溶液显绿色的原因是NO₂ 在溶液中达到饱和,NO₂ 的饱和溶液呈黄色,硝酸铜稀溶液呈蓝色,两者混合后呈绿色。
①甲同学取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是______(用化学方程式表示)。3NO₂ + H₂O = 2HNO₃ + NO
②乙同学认为甲同学所做实验不足以支撑他的推测,还有可能是______。浓硝酸铜溶液是绿色,而稀硝酸铜溶液是蓝色
③丙同学进一步探究反应后溶液呈绿色是否与NO₂ 的溶解有关,设计实验:用不同气体将反应后溶液中的NO₂ 赶出,观察并分析现象。实验记录如下:
注:实验过程中气体流速均已保持一致
实验编号 | 1 | 2 | 3 |
通入气体 | N₂ | CO₂ | O₂ |
实验现象 | 大量红棕色气体逸出,约25min后溶液变为蓝色 | 大量红棕色气体逸出,约25min后溶液变为蓝色 | 大量红棕色气体逸出,约5min后溶液变为蓝色 |
实验2不能将大理石与稀盐酸反应产生的气体直接通入溶液中,请说明原因:______。该实验说明反应后的溶液呈绿色的主要原因______(填“是”或“不是”)的溶解NO₂ 所导致的。
石灰石和稀盐酸制取二氧化碳,盐酸易挥发,制得的中可能存在CO₂气体杂质HCl,通入反应后溶液,Cl-可与铜离子络合生成黄色的四氯合铜离子,影响实验结论;不是(因为NO₂被赶出来后需要25min才变为蓝色,且O₂会加快反应速率,说明O₂参加了变蓝的过程)
(3)丁同学结合上述实验继续推测溶液显绿色源于铜的亚硝酸化合物,铜和浓硝酸的反应过程中,还生成了亚硝酸,进而与铜离子结合形成绿色物质。资料显示为绿色。
①查阅资料后发现尿素[CO(NH3)₂]可以和亚硝酸发生反应但不会影响NO₂ 的生成,在与亚硝酸的反应中可生成两种无污染的气体,其化学方程式为______。
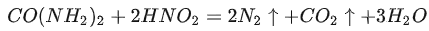
②丙同学往反应结束后的试管中加入一勺尿素,溶液立刻恢复蓝色。随后小组成员又做了补充实验:在铜和浓硝酸反应开始前,提前加入一定量的尿素,反应现象变为______,则说明丁同学的推测具有一定科学性。
在铜和浓硝酸反应开始前加入一定量的尿素,则反应现象变为铜迅速溶解生成大量红棕色气体,溶液变为蓝色,
故答案为:铜迅速溶解,生成大量红棕色气体,溶液变为蓝色。



